حسین سلطانمرادی
حسین سلطانمرادی
تست ProBNP: راهنمای کامل تشخیص و پایش نارسایی قلبی
ProBNP (N-Terminal pro B-Type Natriuretic Peptide) یک نشانگر زیستی مهم در تشخیص و پایش نارسایی قلبی است. این پروتئین بهطور طبیعی توسط قلب ترشح میشود و سطح آن در خون میتواند اطلاعات مهمی درباره سلامت قلب و عملکرد بطنها ارائه دهد. در این مقاله از سایت دکتر ابوئی همراه ما باشید.
عملکرد ProBNP در بدن
هنگامی که قلب تحت فشار قرار میگیرد یا بطنها کشیده میشوند، سلولهای عضلانی قلب پروتئینی به نام BNP ترشح میکنند. BNP به دو شکل در خون ظاهر میشود:
- BNP فعال: فرم عملکردی که به تنظیم فشار خون و دفع مایع از بدن کمک میکند.
- ProBNP یا NT-proBNP: فرم غیر فعال ولی پایدارتر که در خون قابل اندازهگیری است.
اندازهگیری NT-proBNP برای تشخیص نارسایی قلبی کاربرد بیشتری دارد، زیرا سطح آن پایدارتر است و تحت تأثیر تخریب سریع قرار نمیگیرد.
اهمیت تست ProBNP
تست ProBNP یکی از ابزارهای کلیدی در تشخیص و مدیریت بیماریهای قلبی است. از کاربردهای مهم آن میتوان به موارد زیر اشاره کرد:
- تشخیص سریع نارسایی قلبی: سطح بالای ProBNP نشاندهنده افزایش فشار داخل قلب و احتمال نارسایی قلبی است.
- ارزیابی شدت بیماری: میزان ProBNP با شدت نارسایی قلبی ارتباط مستقیم دارد و میتواند روند پیشرفت بیماری را نشان دهد.
- پایش درمان: کاهش سطح ProBNP پس از شروع درمان نشاندهنده بهبود عملکرد قلب است و پزشک میتواند اثربخشی داروها و تغییر سبک زندگی را ارزیابی کند.
- تفکیک علل تنگی نفس: در افرادی که دچار تنگی نفس هستند، این تست به پزشک کمک میکند تشخیص دهد آیا علت قلبی دارد یا مشکلات ریوی یا دیگر بیماریها.
چه زمانی باید تست ProBNP انجام داد؟
تست ProBNP معمولاً زمانی درخواست میشود که بیمار علائم زیر را داشته باشد:
- تنگی نفس یا احساس خستگی سریع هنگام فعالیت
- تورم در پاها، مچها یا شکم
- افزایش وزن ناگهانی
- درد قفسه سینه یا ضربان قلب نامنظم
همچنین این تست در افرادی که سابقه نارسایی قلبی دارند، برای پایش وضعیت قلب توصیه میشود.
نحوه انجام تست
تست ProBNP یک آزمایش خون ساده است که معمولاً در آزمایشگاه انجام میشود:
- نمونهگیری خون: خون از ورید بازو گرفته میشود.
- اندازهگیری در آزمایشگاه: نمونه با روشهای اختصاصی مانند ELISA یا دستگاههای خودکار بررسی میشود.
- تفسیر نتایج: پزشک با توجه به سطح ProBNP، سن، جنسیت و شرایط پزشکی بیمار، نتیجه را ارزیابی میکند.
تفسیر نتایج
تفسیر نتایج باید توسط پزشک انجام شود، اما به طور کلی:
| سطح NT-proBNP | تفسیر کلی |
|---|---|
| پایین | عملکرد قلب طبیعی است |
| متوسط | نیاز به بررسی بیشتر و انجام آزمایشهای تکمیلی |
| بالا | احتمال نارسایی قلبی یا فشار بالای قلب و نیاز به درمان فوری |
توجه: سطح ProBNP ممکن است تحت تأثیر سن، جنسیت، بیماریهای کلیوی و برخی داروها قرار گیرد. بنابراین همیشه باید با پزشک مشورت شود.
عوامل مؤثر بر سطح ProBNP
- سن و جنسیت: افراد مسن و زنان ممکن است سطح بالاتری داشته باشند.
- بیماریهای کلیوی: کاهش عملکرد کلیه میتواند سطح ProBNP را افزایش دهد.
- چاقی: افراد دارای اضافه وزن ممکن است سطح ProBNP کمی پایینتر داشته باشند.
- داروها: برخی داروهای قلبی و فشار خون میتوانند سطح ProBNP را تغییر دهند.
مزایای انجام تست در آزمایشگاه معتبر
انجام تست ProBNP در یک آزمایشگاه تخصصی مانند رادمان فردیس مزایای زیادی دارد:
- استفاده از دستگاههای پیشرفته و دقیق برای اندازهگیری سطح ProBNP
- تیم متخصص و با تجربه برای نمونهگیری و تفسیر نتایج
- ارائه نتایج سریع و قابل اعتماد برای تشخیص و پایش درمان
- امکان ارائه مشاوره تخصصی جهت مراحل بعدی درمان
جمعبندی
تست ProBNP یک ابزار حیاتی در تشخیص و پایش نارسایی قلبی است. انجام این آزمایش به موقع میتواند از پیشرفت بیماری جلوگیری کند، درمان مناسب را مشخص کند و کیفیت زندگی بیماران را بهبود دهد. برای انجام تست ProBNP با بالاترین دقت و دریافت مشاوره تخصصی، آزمایشگاه رادمان فردیس آماده خدمترسانی به شماست.
تأثیر کاکائو بر تنبلی تخمدان؛ آیا کاکائو باعث ایجاد PCOS میشود؟
تأثیر کاکائو بر تنبلی تخمدان یکی از موضوعاتی است که میان بسیاری از زنان و حتی برخی متخصصان مراقبتهای سلامت، باعث ایجاد پرسش و گاهی سردرگمی میشود. برخی تصور میکنند کاکائو یا شکلات میتواند موجب بروز سندروم تخمدان پلیکیستیک (PCOS) شود، در حالی که شواهد علمی تصویر بسیار متفاوتی ارائه میدهند. در این مقاله، برای خوانندگان وبسایت دکتر ابوئی، بهصورت علمی، دقیق و با رعایت اصول سئو توضیح میدهیم که آیا کاکائو واقعاً برای تخمدانها مضر است یا خیر، و کدام شکل مصرفی آن ممکن است علائم PCOS را تشدید کند.
کاکائو چیست و چرا درباره آن اختلاف نظر وجود دارد؟
کاکائو مادهای خام و سرشار از آنتیاکسیدانها، فلاوانولها و منیزیم است؛ موادی که اغلب با کاهش التهاب، بهبود متابولیسم و تنظیم بهتر هورمونها همراه هستند.
اما مشکل اصلی از جایی شروع میشود که بسیاری از افراد بهجای «کاکائوی خالص»، شکلاتهای صنعتی شیرین را با کاکائو اشتباه میگیرند. این شکلاتها سرشار از قند، چربیهای ناسالم و کالری بالا هستند؛ سه عاملی که میتوانند مقاومت به انسولین را تشدید کنند و وضعیت متابولیک بیماران مبتلا به تنبلی تخمدان را بدتر سازند.
به همین دلیل برخی متخصصان مانند ماماها از روی تجربه بالینی میگویند «کاکائو برای PCOS خوب نیست»، در حالی که مشکل کاکائو نیست؛ قند بالای شکلاتهای صنعتی است.
آیا کاکائوی خالص باعث تنبلی تخمدان میشود؟
طبق مطالعات معتبر علمی:
✔️ کاکائوی خالص موجب ایجاد PCOS نمیشود
✔️ هیچ پژوهشی نشان نداده کاکائو عامل اختلالات هورمونی یا چربیهای شکمی است
✔️ کاکائو نه تنها مضر نیست، بلکه در صورت مصرف درست میتواند اثرات حمایتی متابولیکی داشته باشد
PCOS یک بیماری چندعاملی است و علل اصلی آن شامل موارد زیر است:
- زمینه ژنتیکی
- مقاومت به انسولین
- التهاب مزمن
- اضافهوزن
- استرس
- تغذیه نامناسب و پرقند
در هیچکدام از این فهرستها «کاکائوی خالص» به عنوان عامل بیماری مطرح نشده است.
کدام نوع کاکائو برای زنان مبتلا به تنبلی تخمدان مضر است؟
❌ شکلات شیرین و صنعتی
- قند بالا
- چربیهای ترانس
- افزودنیها
- کالری زیاد
همین ترکیبات میتوانند باعث شوند علائم PCOS مانند مقاومت به انسولین، جوش، افزایش وزن و بینظمی دورهها تشدید شود. بنابراین توصیه به پرهیز از «کاکائو» در واقع توصیه به پرهیز از شکلاتهای صنعتی است.
✔️ کاکائوی خالص یا شکلات تلخ واقعی (بالای ۷۰٪)
این دسته از محصولات:
- قند بسیار کمی دارند
- حاوی آنتیاکسیدانهای مفید هستند
- التهاب را کاهش میدهند
- بر حساسیت انسولینی اثر مثبت دارند
در نتیجه برای افراد مبتلا به PCOS میتوانند انتخاب مناسبی باشند.
خواص مفید کاکائوی خالص برای بیماران مبتلا به PCOS
۱. کاهش التهاب سیستمیک
التهاب مزمن یکی از ویژگیهای رایج در تنبلی تخمدان است. پلیفنولهای کاکائو با کاهش استرس اکسیداتیو میتوانند به بهبود تعادل هورمونی کمک کنند.
۲. بهبود مقاومت به انسولین
بخش بزرگی از بیماران مبتلا به PCOS مقاومت به انسولین دارند.
فلاوانولهای کاکائو در مطالعات مختلف باعث:
- کاهش قند ناشتا
- بهبود پاسخ انسولینی
- تنظیم بهتر متابولیسم
شدهاند.
۳. بهبود خلق و کاهش استرس
کاکائو سطح دوپامین و سروتونین را افزایش میدهد و این موضوع میتواند برای بیمارانی که به دلیل اختلالات هورمونی دچار اضطراب یا افسردگی میشوند مفید باشد.
در مسیر تشخیص و کنترل تنبلی تخمدان، انجام آزمایشهای دقیق هورمونی و متابولیک اهمیت بسیار زیادی دارد.
در این زمینه، آزمایشگاه رادمان با استفاده از تجهیزات پیشرفته، دقت بالا در نتایج و امکان دریافت آنلاین گزارشها، یکی از بهترین مراکز برای انجام آزمایشهای مرتبط با هورمونهای زنانه، تست مقاومت به انسولین، چکاپ PCOS، پروفایل قند و چربی و سایر تستهای ضروری برای بیماران است.
رادمان برای مراجعان بهویژه بانوانی که تحت نظر دکتر ابوئی هستند، میتواند یک گزینه قابل اعتماد برای انجام آزمایشهای دورهای باشد.
آیا باید مصرف کاکائو را قطع کنیم؟
پاسخ علمی ساده است:
✔️ مصرف کاکائوی خالص یا شکلات تلخ: بلامانع و حتی مفید
❌ مصرف شکلاتهای صنعتی و پرقند: مضر و تشدیدکننده علائم
چگونه کاکائو را سالم مصرف کنیم؟
- استفاده از پودر کاکائوی خالص در اسموتی یا شیر کمچرب
- مصرف روزانه ۱۰ تا ۲۰ گرم شکلات تلخ واقعی
- پرهیز از شکلاتهای شیری و محصولات کاکائویی پرقند
- مطالعه برچسب مواد غذایی قبل از خرید
جمعبندی نهایی
«کاکائو» بهخودیخود نه تنها موجب تنبلی تخمدان نمیشود، بلکه در صورت انتخاب نوع مناسب میتواند به کاهش التهاب، بهبود متابولیسم و تنظیم بهتر هورمونها کمک کند. برخلاف باورهای رایج، این قند و چربی بالای شکلاتهای صنعتی است—not کاکائوی خالص—که میتواند برای بیماران مبتلا به PCOS مشکلساز باشد.
برای زنان مبتلا به تنبلی تخمدان، انتخاب درست میان کاکائوی خالص و شکلاتهای صنعتی تفاوتی اساسی ایجاد میکند؛ تفاوتی که در کنار نظارت پزشکی و آزمایشهای دورهای، به مدیریت بهتر این بیماری کمک خواهد کرد.
محافظت از بدن در برابر آلودگی هوا
در این مقاله از سایت دکتر ابوئی به بررسی موضوع محافظت در برابر آلودگی هوا میپردازیم. در سالهای اخیر، شایعاتی مانند «کمتریل» (Chemtrail) در فضای مجازی بسیار پخش شدهاند؛ شایعاتی که ادعا میکنند خطوط سفید پشت هواپیماها حاوی مواد شیمیایی خطرناک عمدی هستند. این باورها پایه علمی و شواهد معتبر ندارند و با یافتههای هواشناسی و فیزیک جو سازگار نیستند.
اما گسترش چنین شایعاتی نشان میدهد که نگرانی مردم درباره آلودگی هوا واقعی و جدی است. به همین دلیل تصمیم گرفتیم این مقاله را بنویسیم تا به جای پرداختن به روایتهای بدون پشتوانه، راههای علمی و معتبر محافظت از بدن در برابر آلودگی هوا را ارائه کنیم.
مراقبت از سیستم تنفسی
استفاده از ماسکهای مناسب
- ماسکهای N95 یا FFP2 بیشترین میزان فیلتر ذرات ریز را دارند.
- ماسک باید کاملاً فیت صورت باشد.
- ماسکهای پارچهای معمولی برای هوای آلوده مناسب نیستند.
کاهش فعالیت بدنی سنگین در فضای باز
ورزش سنگین در روزهای آلوده باعث ورود حجم بیشتری از آلایندهها به ریه میشود. فعالیتها را در فضای سرپوشیده و دارای تهویه مناسب انجام دهید.
تقویت سیستم ایمنی و کاهش التهاب
تغذیه غنی از آنتیاکسیدان
مواد غذایی زیر به کاهش اثرات استرس اکسیداتیو ناشی از آلودگی کمک میکنند:
- انار، تمشک، بلوبری
- اسفناج، بروکلی و سبزیجات برگتیره
- بادام، گردو و تخمهها
- زردچوبه، زنجبیل و دارچین
مصرف آب کافی
هیدراته ماندن به دفع بهتر ذرات و رقیق شدن ترشحات مخاطی کمک میکند.
ایجاد محیط امن در خانه
استفاده از دستگاه تصفیه هوا
دستگاههای دارای فیلتر HEPA قادرند ذرات معلق و آلایندههای درشتتر را حذف کنند.
فیلتر باید طبق دستور کارخانه بهروز و تعویض شود.
تهویه کنترلشده
در روزهای با شاخص آلودگی بهتر، پنجرهها را باز کنید؛ اما در روزهای بسیار آلوده، پنجرهها را بسته نگه دارید و درزها را تا حد امکان مسدود کنید.
مراقبت از سلامت قلب و عروق
آلودگی هوا میتواند موجب التهاب عروقی و تشدید بیماریهای قلبی شود. راهکارهای مهم:
- فعالیت بدنی منظم در محیط امن
- رژیم غذایی سالم شامل ماهی، روغن زیتون و سبزیجات
- مدیریت استرس و خواب کافی
استفاده از اپلیکیشنهای پایش آلودگی
چک کردن شاخص کیفیت هوا (AQI) قبل از خروج از خانه، یکی از مهمترین اقدامات پیشگیرانه است.
- زیر ۱۰۰: قابل قبول
- ۱۵۰ به بالا: خطرناک برای گروههای حساس
- ۲۰۰ به بالا: برای همه گروهها ناسالم
راهکارهای مخصوص گروههای حساس
کودکان
به دلیل راههای هوایی کوچکتر و رشد ریه، آسیبپذیری بیشتری دارند.
در روزهای آلوده از بازی طولانی در فضای باز جلوگیری کنید.
سالمندان و بیماران قلبی–ریوی
- از قرارگیری در بیرون در روزهای بالای ۱۵۰ اجتناب کنند.
- داروها را طبق نسخه پزشک بهطور منظم مصرف کنند.
اشاره به ویدئوهای آهنربا و گرد و غبار: واقعیت علمی چیست؟
در ماههای اخیر کلیپهایی در فضای مجازی منتشر شده که در آن افراد گرد و غبار روی خودرو را جمع میکنند و سپس با نزدیککردن آهنربا، مشاهده میکنند که بخشی از این ذرات به آهنربا میچسبد. در این ویدئوها ادعا میشود این پدیده «مدرک وجود کمتریل» یا پاشیدن عمدی مواد فلزی از آسمان است.
اما این برداشت از نظر علمی صحیح نیست و پدیدهای که در این ویدئوها دیده میشود، علتهای شناختهشده، طبیعی و صنعتی دارد:
وجود ذرات آهن و اکسیدهای آهن در گرد و غبار
در بسیاری از مناطق، بخشی از گرد و غبار طبیعی شامل ذرات ریز آهن یا اکسید آهن (مانند مگنتیت) است. این ذرات مغناطیسیاند و وجودشان کاملاً طبیعی و وابسته به ترکیب خاک همان منطقه است.
در روزهایی که باد شدید یا ریزگردها افزایش مییابد، این ذرات بیشتر نمایان میشوند.
منشأ شهری و صنعتی
در شهرها، یکی از مهمترین منابع ذرات مغناطیسی:
- سایش لنت ترمز خودروها
- ذرات ناشی از فعالیتهای صنعتی
- سوزاندن سوختهای فسیلی
است.
ذرات فلزی حاصل از این فرایندها نیز به آهنربا جذب میشوند و کاملاً مستقل از شایعه کمتریل هستند.
افزایش آلودگی هوای شهری = افزایش ذرات فلزی
در کلانشهرهایی با ترافیک سنگین و صنایع نزدیک، طبیعی است که میزان ذرات فلزی در هوا بالاتر باشد. چنین ذراتی هیچ ارتباطی با پاشیدن عمدی مواد از هواپیما ندارند و در واقع یکی از شاخصهای شناختهشده آلودگی هوا محسوب میشوند.
خطوط سفید پشت هواپیما و ارتباط اشتباه با این پدیده
این ویدئوها معمولاً به شکل غیرعلمی، چسبیدن گرد و غبار به آهنربا را با خطوط سفید پشت هواپیماها مرتبط میکنند؛ در حالی که آن خطوط در واقع کنتریل (Contrail) هستند—بخار آب یخزده حاصل از اختلاف دما و فشار—و هیچ ارتباطی با انتشار مواد فلزی ندارند.
جمعبندی علمی درباره کلیپهای آهنربا
چسبیدن برخی ذرات گرد و غبار به آهنربا:
- پدیدهای طبیعی و شناختهشده است
- ناشی از وجود ذرات آهن، اکسید آهن یا ذرات فلزی شهری است
- مدرکی برای وجود کمتریل یا پاشیدن مواد از آسمان نیست
جمعبندی
با وجود رواج شایعات درباره آلودگی هوا، آنچه واقعاً اهمیت دارد اطلاعات علمی و اقدامات کاربردی برای حفظ سلامت است. استفاده از ماسک مناسب، تقویت ایمنی با تغذیه سالم، بهبود کیفیت هوای داخل خانه و پایش دائم شاخص آلودگی میتوانند تأثیر قابلتوجهی بر کاهش آسیبهای آلودگی هوا داشته باشند.
در همین راستا، آزمایشگاه رادمان فردیس با بهرهگیری از تجهیزات بهروز و پرسنل متخصص، امکان انجام آزمایشهای مرتبط با سلامت عمومی، بررسی شاخصهای التهابی را فراهم کرده است. این مرکز با ارائه خدمات دقیق و قابل اعتماد، محیطی مطمئن برای افرادی است که میخواهند از وضعیت سلامت خود آگاه شوند یا نتایج آزمایشهای دورهایشان را پیگیری کنند. اگر در روزهای آلوده به دنبال ارزیابی وضعیت بدنی خود هستید، مراجعه به رادمان فردیس میتواند گام مهمی در مسیر مراقبت از سلامتتان باشد.
تشخیص افتراقیهای فارنژیت (Differential Diagnosis of Pharyngitis)
فارنژیت (Pharyngitis) به التهاب حاد یا مزمن مخاط حلق گفته میشود و یکی از شایعترین علل گلودرد (Sore throat) در بیماران سرپایی است. این بیماری میتواند ناشی از عوامل عفونی (ویروسی، باکتریایی یا قارچی) و یا عوامل غیرعفونی مانند آلرژی، ریفلاکس یا تحریکات محیطی باشد.
تشخیص دقیق علت، نه تنها برای انتخاب درمان مناسب بلکه برای پیشگیری از مصرف بیمورد آنتیبیوتیکها و عوارض بعدی مانند تب روماتیسمی حاد (Acute Rheumatic Fever) اهمیت حیاتی دارد. در این مقاله از سایت دکتر ابوئی به بررسی تشخیص افتراقیهای فارنژیت میپردازیم. در ادامه همراه ما باشید.
فارنژیت ویروسی (Viral Pharyngitis)
شیوع و پاتوژنز
حدود ۷۰ تا ۸۰ درصد موارد فارنژیت در بالغین و کودکان منشأ ویروسی دارند. انتقال معمولاً از طریق قطرات تنفسی یا تماس مستقیم با ترشحات آلوده صورت میگیرد.
ویروسهای شایع
- آدنوویروس (Adenovirus)
- راینوویروس (Rhinovirus)
- ویروس آنفلوآنزا و پاراآنفلوآنزا
- ویروس اپشتینبار (EBV) – عامل مونونوکلئوز عفونی
- ویروس هرپس سیمپلکس (HSV-1)
تظاهرات بالینی
- شروع تدریجی گلودرد
- تب خفیف تا متوسط
- سرفه، رینوره، گرفتگی بینی
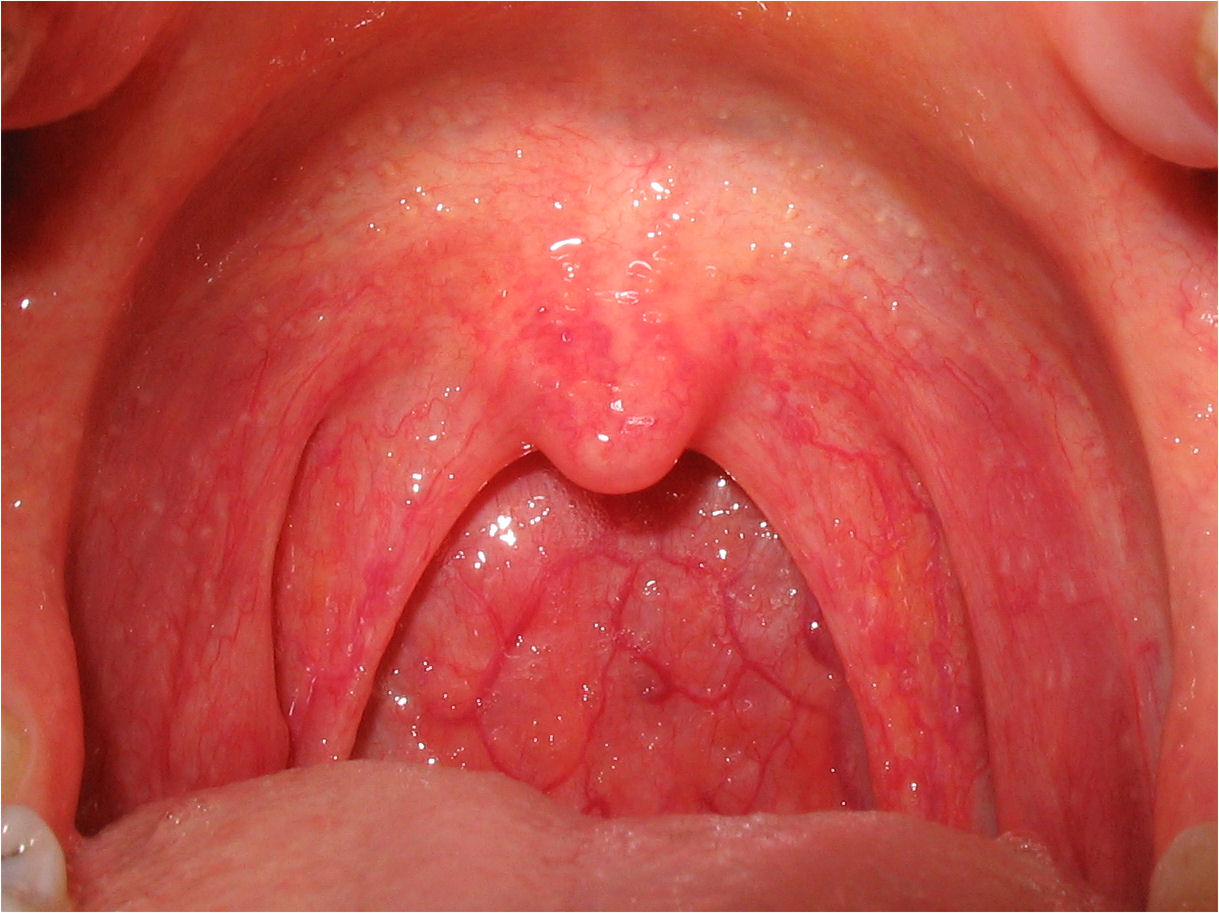
- گلودرد خفیف با اریتم حلق بدون ترشحات چرکی
- در موارد EBV: لنفادنوپاتی خلفی گردن، بزرگی طحال و خستگی شدید
نکات افتراقی مهم
وجود سرفه، کونژکتیویت و رینوره معمولاً علیه فارنژیت باکتریایی و به نفع منشاء ویروسی است.
فارنژیت باکتریایی (Bacterial Pharyngitis)
عامل شایع
استرپتوکوک گروه A (Group A Streptococcus; GAS) مسئول حدود ۱۵–۳۰٪ موارد در کودکان و ۵–۱۰٪ در بالغین است.
پاتوفیزیولوژی
تولید استرپتوکیناز، هیالورونیداز و اگزوتوکسینها منجر به التهاب شدید مخاط و پاسخ ایمنی میزبان میشود که میتواند عوارض سیستمیک ایجاد کند.
تظاهرات بالینی
- شروع ناگهانی گلودرد شدید
- تب بالا (>۳۸٫۵°C)
- عدم وجود سرفه
- ترشحات چرکی یا نقاط سفید روی لوزهها
- لنفادنوپاتی دردناک گردنی قدامی
- در برخی بیماران: راش اریتروماتوز منتشر (اسکارلتینا)
سایر علل باکتریایی کمتر شایع
- استرپتوکوک گروه C و G
- نایسریا گونورهآ (Gonococcal pharyngitis) – در تماس جنسی دهانی
- کورینهباکتریوم دیفتریا – ایجاد غشای ضخیم خاکستریرنگ در حلق
- مایکوپلاسما پنومونیه و کلامیدوفیلا پنومونیه – بیشتر در نوجوانان
معیارهای تشخیصی بالینی (Centor Score)
- تب بالای ۳۸°C
- عدم وجود سرفه
- ترشح چرکی لوزهها
- لنفادنوپاتی گردنی قدامی
- سن بیمار (افزایش خطر در کودکان)
امتیاز ≥۳ نیاز به انجام تست سریع آنتیژن یا کشت گلو دارد.
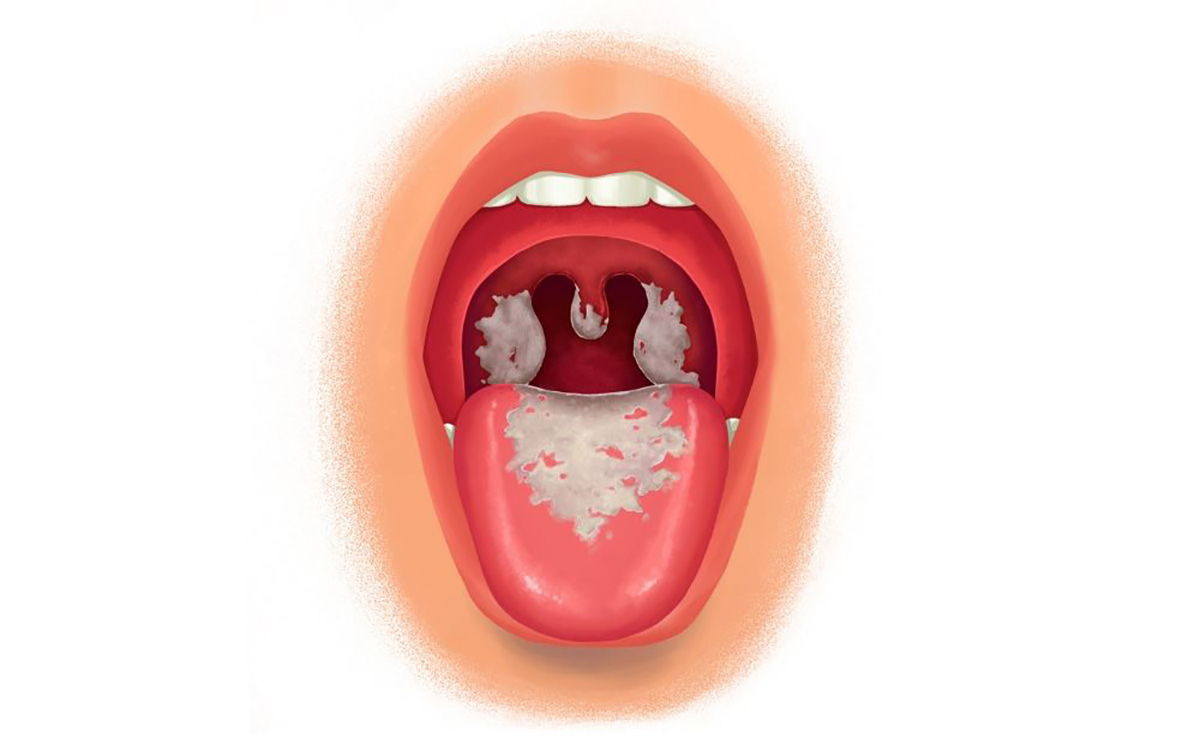
فارنژیت قارچی (Fungal Pharyngitis)
علت
اغلب ناشی از کاندیدا آلبیکانس است، خصوصاً در بیماران با ایمنی سرکوبشده، دیابت، یا مصرف طولانی آنتیبیوتیک و کورتیکواستروئید.
علائم
- وجود پلاکهای سفید قابل برداشت روی مخاط حلق و زبان
- سوزش و دیسفاژی خفیف
- در موارد شدید، درگیری مری (Candidal esophagitis)
فارنژیت غیرعفونی (Noninfectious Pharyngitis)
الف) علل تحریککننده محیطی
- دود سیگار، آلودگی هوا، گازهای شیمیایی
- خشکی هوا، فریاد زدن یا استفاده بیش از حد از صدا
ب) آلرژی (Allergic Pharyngitis)
- خارش و تحریک گلو، عطسه و رینوره شفاف
- معمولاً بدون تب یا لنفادنوپاتی
ج) ریفلاکس معدی-مروی (GERD)
- گلودرد مزمن بهویژه صبحها
- احساس جسم خارجی در گلو
- ارتباط با سوزش سر دل و برگشت اسید
بیماریهایی با تظاهر مشابه فارنژیت
| بیماری | ویژگی افتراقی کلیدی |
|---|---|
| مونونوکلئوز عفونی (EBV) | لنفادنوپاتی خلفی، بزرگی طحال، تست Monospot مثبت |
| دیفتری | غشای ضخیم خاکستری، بوی بد دهان، خطر خفگی |
| آبسه پریتونسیلار | گلودرد یکطرفه، تریسموس، انحراف زبان کوچک |
| آبسه رتروفارنژیال | درد گردن، محدودیت حرکات، تب بالا |
| ریفلاکس معدی-مروی | گلودرد مزمن بدون علائم عفونی |
| فارنژیت آلرژیک | خارش و ترشحات شفاف بینی بدون تب |
روشهای تشخیصی
- شرح حال دقیق و معاینه بالینی حلق و لوزهها
- Rapid Antigen Detection Test (RADT) برای GAS – حساسیت ۷۰–۹۰٪
- کشت گلو (Throat culture) – استاندارد طلایی در تشخیص استرپتوکوکی
- CBC: لنفوسیتوز در عفونت ویروسی، نوتروفیلی در باکتریایی
- Monospot test یا Anti-EBV antibodies در موارد مشکوک به EBV
- آندوسکوپی یا pH متریک در موارد مشکوک به GERD
درمان بر اساس علت
| نوع فارنژیت | درمان اصلی |
|---|---|
| ویروسی | درمان حمایتی: استراحت، مایعات گرم، ضدتبها |
| باکتریایی (GAS) | پنیسیلین V یا آموکسیسیلین ۱۰ روزه |
| آلرژیک | آنتیهیستامین، پرهیز از آلرژن |
| قارچی | نیستاتین یا فلوکونازول |
| ریفلاکس | مهارکننده پمپ پروتون، تغییر سبک زندگی |
جمعبندی
فارنژیت یک تظاهر بالینی چندعاملی است که تشخیص افتراقی دقیق آن نیازمند ارزیابی جامع بالینی، آزمایشگاهی و در صورت لزوم تصویربرداری است. افتراق بین فارنژیت استرپتوکوکی و فارنژیت ویروسی از نظر درمانی حیاتی است؛ چراکه درمان نابجای آنتیبیوتیکی نه تنها سودمند نیست بلکه به مقاومت میکروبی میانجامد.
آشنایی دانشجویان پزشکی با الگوهای بالینی و پاتوفیزیولوژی هر نوع فارنژیت، گامی اساسی در ارتقاء کیفیت تشخیص و درمان بیماران است.
بیماریهایی که از طریق بوسیدن منتقل میشوند | راههای پیشگیری و دانستنیهای پزشکی
شوند | راههای پیشگیری و دانستنیهای پزشکی
بوسیدن یکی از صمیمانهترین رفتارهای انسانی است که نقش مهمی در ایجاد ارتباط عاطفی دارد. با این حال، تماس مستقیم دهان با دهان یا پوست دیگران میتواند مسیر انتقال برخی از عفونتهای ویروسی و باکتریایی باشد. در این مقاله از سایت دکتر ابوئی، به بررسی علمی بیماریهایی که از طریق بوسیدن منتقل میشوند، راههای پیشگیری، و پاسخ به پرسشهای متداول در این زمینه میپردازیم.
🔬 چرا بوسیدن میتواند موجب انتقال بیماری شود؟
بزاق دهان حاوی میلیونها میکروارگانیسم (ویروس، باکتری و قارچ) است. در حالت عادی، بیشتر آنها برای بدن بیضررند، اما برخی از آنها در شرایط خاص یا هنگام تماس مستقیم دهان با دهان میتوانند وارد بدن فرد مقابل شده و بیماری ایجاد کنند.
عوامل مؤثر در احتمال انتقال بیماری از طریق بوسه عبارتاند از:
- وجود زخم، تبخال یا التهاب در دهان
- ضعف سیستم ایمنی
- وجود خون در بزاق (بهویژه در بیماریهای لثه)
- تماس طولانیمدت و نزدیک دهانی
🦠 بیماریهای ویروسی منتقلشونده از طریق بوسیدن
ویروس هرپس سیمپلکس نوع ۱ (HSV-1)
این ویروس عامل اصلی تبخال لب است و یکی از شایعترین عفونتهای منتقلشونده از طریق بوسه به شمار میرود.
- 🔹 راه انتقال: تماس مستقیم با تاول یا بزاق فرد آلوده
- 🔹 علائم: تاولهای دردناک روی لب یا اطراف دهان، سوزش، تب خفیف
- 🔹 پیشگیری: پرهیز از بوسیدن در هنگام وجود زخم فعال یا حتی احساس سوزش اولیه
نکته: ویروس هرپس حتی در زمانی که ضایعه قابل مشاهده نیست نیز ممکن است از طریق بزاق منتقل شود.
مونونوکلئوز عفونی (Mononucleosis) – “بیماری بوسه”
این بیماری توسط ویروس اپشتینبار (Epstein-Barr Virus) ایجاد میشود.
- 🔹 راه انتقال: بزاق، تماس دهانی
- 🔹 علائم: تب، گلودرد شدید، خستگی مفرط، تورم غدد لنفاوی
- 🔹 پیشگیری: پرهیز از تماس دهانی با فردی که علائم گلودرد یا تب دارد
سیتومگالوویروس (Cytomegalovirus – CMV)
از خانواده ویروسهای هرپس است و در افراد سالم معمولاً بیعلامت باقی میماند، اما برای نوزادان و بیماران با نقص ایمنی خطرناک است.
- 🔹 راه انتقال: بزاق، خون، ادرار، تماس جنسی
- 🔹 پیشگیری: رعایت بهداشت، شستوشوی دستها، پرهیز از تماس دهانی در زمان بیماری
ویروسهای تنفسی (سرماخوردگی، آنفلوآنزا، کرونا، RSV)
بوسیدن میتواند باعث انتقال ویروسهای دستگاه تنفسی شود.
- 🔹 راه انتقال: قطرات بزاق، عطسه و سرفه
- 🔹 پیشگیری: خودداری از تماس نزدیک در زمان بیماری، تهویه مناسب محیط
🧫 بیماریهای باکتریایی و عفونتهای دهانی
انتقال باکتریهای دهانی
باکتریهای عامل پوسیدگی دندان و بیماریهای لثه میتوانند از فردی به فرد دیگر منتقل شوند.
- 🔹 پیشگیری: رعایت بهداشت دهان، مراجعه منظم به دندانپزشک، استفاده از مسواک شخصی
مننژوکوک (عامل مننژیت باکتریایی)
اگرچه نادر است، اما ممکن است از طریق بزاق منتقل شود، بهویژه در تماسهای نزدیک و طولانیمدت.
- 🔹 پیشگیری: واکسیناسیون و رعایت بهداشت فردی
هپاتیت B
احتمال انتقال از طریق بزاق بسیار پایین است، ولی در صورتی که فرد مبتلا دارای زخم یا خونریزی دهانی باشد، ریسک افزایش مییابد.
- 🔹 پیشگیری: واکسیناسیون هپاتیت B و اجتناب از تماس با ترشحات آلوده
🧠 نکات پیشگیرانه در بوسیدن سالم
✅ در زمان تبخال فعال، زخم یا التهاب دهانی از بوسیدن خودداری کنید.
✅ مسواک، لیوان و رژ لب خود را با کسی به اشتراک نگذارید.
✅ در صورت ابتلا به بیماریهای تنفسی یا تبدار، تماس دهانی را محدود کنید.
✅ برای حفظ سلامت دهان، از دهانشویههای آنتیسپتیک استفاده کنید.
✅ اگر سیستم ایمنی ضعیفی دارید (مثلاً در اثر دیابت، مصرف داروهای تضعیفکننده ایمنی، یا HIV)، احتیاط بیشتری کنید.
❓ سوالات متداول درباره انتقال بیماری از طریق بوسیدن
🔸 آیا بوسیدن روی گونه هم خطر دارد؟
خیر، در بیشتر موارد بوسهی روی گونه ایمن است، مگر اینکه فرد مقابل زخم یا تبخال فعال داشته باشد.
🔸 آیا تبخال درمان قطعی دارد؟
خیر، ویروس هرپس در بدن باقی میماند و ممکن است در مواقع ضعف ایمنی دوباره فعال شود. درمانها فقط به کاهش علائم و دفعات عود کمک میکنند.
🔸 آیا امکان انتقال HIV از طریق بوسیدن وجود دارد؟
خیر، ویروس HIV از طریق بوسه منتقل نمیشود مگر در شرایط بسیار نادر که زخمهای باز و خون قابل مشاهده در دهان هر دو نفر وجود داشته باشد.
🔸 کودکان چطور در معرض خطرند؟
سیستم ایمنی کودکان هنوز کامل نشده است؛ بنابراین بهتر است در زمان بیماری از بوسیدن صورت یا دهان کودک پرهیز شود.
🔸 بهترین راه پیشگیری چیست؟
رعایت بهداشت دهان، اجتناب از بوسیدن هنگام بیماری، واکسیناسیون (برای هپاتیت B و مننژوکوک) و آگاهی از وضعیت سلامتی فرد مقابل.
📚 جمعبندی
بوسیدن، اگرچه رفتاری انسانی و طبیعی است، اما میتواند مسیر انتقال برخی عفونتها باشد. رعایت بهداشت فردی و پرهیز از بوسه در زمان بیماری، بهترین راه برای حفظ سلامت خود و عزیزانتان است. آگاهی و پیشگیری، مهمترین ابزار در برابر بیماریها هستند.
تست سل فری دیانای (cfDNA) یا NIPT چیست؟
تست سل فری دیانای که با نام NIPT (Non-Invasive Prenatal Test) نیز شناخته میشود، یکی از جدیدترین و دقیقترین روشهای غربالگری پیش از تولد است. این آزمایش با بررسی قطعات کوچکی از DNA جنینی که در خون مادر وجود دارد، احتمال ابتلا جنین به برخی از اختلالات کروموزومی شایع را مشخص میکند؛ بدون اینکه نیازی به نمونهبرداری مستقیم از رحم یا جنین باشد. در ادامه ی این مقاله از سایت دکتر ابوئی همراه ما باشید.
ماهیت و نحوه عملکرد تست cfDNA
در دوران بارداری، بخشی از سلولهای جفت (Placenta) که از نظر ژنتیکی با جنین یکسان هستند، میمیرند و قطعاتی از DNA آنها وارد جریان خون مادر میشود. این قطعات بهصورت آزاد در پلاسما شناورند و به آنها سل فری دیانای (Cell-free DNA) گفته میشود.
در تست NIPT، با گرفتن یک نمونه خون ساده از مادر، این DNA استخراج و با روشهای پیشرفته ژنتیکی مورد تجزیه و تحلیل قرار میگیرد تا مشخص شود که آیا تعداد کروموزومهای خاصی در DNA جنین بیش از حد معمول (تریزومی) است یا خیر.
هدف انجام تست
تست cfDNA برای غربالگری برخی از شایعترین ناهنجاریهای کروموزومی به کار میرود، از جمله:
- تریزومی ۲۱ (سندرم داون)
- تریزومی ۱۸ (سندرم ادوارد)
- تریزومی ۱۳ (سندرم پاتو)
- در برخی نسخهها، بررسی اختلالات کروموزومهای جنسی (X و Y) مانند سندرم ترنر یا کلاینفلتر
- تعیین جنسیت جنین (در صورت درخواست والدین)
زمان مناسب برای انجام تست
بهترین زمان انجام تست NIPT از هفته دهم بارداری به بعد است.
در این مرحله، مقدار cfDNA جنینی در خون مادر به اندازه کافی بالا رفته و نتیجه تست با دقت قابل اعتماد گزارش میشود.
دقت تست NIPT چقدر است؟
یکی از مزیتهای مهم تست سل فری دیانای، دقت بسیار بالا در شناسایی اختلالات کروموزومی است:
- دقت برای سندرم داون (تریزومی ۲۱) بیش از ۹۹٪
- دقت برای تریزومی ۱۸ و ۱۳ حدود ۹۷ تا ۹۹٪
اما باید توجه داشت که NIPT یک تست غربالگری است، نه تشخیصی. به این معنا که اگر نتیجه مشکوک یا مثبت شود، حتماً باید برای تأیید نهایی از روشهای تشخیصی مانند آمنیوسنتز یا نمونهگیری از پرزهای جفتی (CVS) استفاده شود.
مزایای تست سل فری دیانای
- ✅ غیرتهاجمی و ایمن – فقط با نمونهگیری خون مادر انجام میشود و هیچ خطری برای جنین ندارد.
- ✅ دقت بسیار بالا – بالاترین دقت در میان تستهای غربالگری پیش از تولد.
- ✅ قابل انجام در اوایل بارداری – از هفته ۱۰ به بعد.
- ✅ کاهش نیاز به تستهای تهاجمی – بسیاری از مادران با نتیجه طبیعی NIPT نیازی به آمنیوسنتز پیدا نمیکنند.
- ✅ بررسی اختلالات جنسی و تعیین جنسیت جنین (در صورت تمایل والدین).
محدودیتها و نکات قابل توجه
- NIPT نمیتواند تمامی اختلالات ژنتیکی یا ساختاری را تشخیص دهد.
- در برخی موارد، ممکن است میزان cfDNA جنینی در خون مادر کم باشد (بهویژه در بارداریهای زودتر از هفته ۱۰ یا مادران با اضافهوزن بالا) و نتیجه “غیرقابل تفسیر” اعلام شود.
- در بارداریهای چندقلویی، دقت تست کمی کاهش مییابد.
- تست نتیجه قطعی ارائه نمیدهد؛ در صورت مثبت شدن نتیجه، حتماً باید بررسی تشخیصی انجام شود.
تفاوت تست NIPT با آمنیوسنتز
| ویژگی | NIPT (سل فری دیانای) | آمنیوسنتز |
|---|---|---|
| نوع تست | غربالگری (احتمال وجود ناهنجاری) | تشخیصی (قطعی) |
| روش انجام | نمونه خون مادر | نمونهگیری از مایع آمنیوتیک |
| خطر برای جنین | ندارد | احتمال بسیار کم سقط (حدود ۰٫۱٪) |
| زمان انجام | از هفته ۱۰ بارداری به بعد | معمولاً هفتههای ۱۵ تا ۲۰ |
| دقت | بسیار بالا ولی نه قطعی | ۱۰۰٪ (برای اختلالات بررسیشده) |
چه کسانی بیشتر از دیگران به NIPT توصیه میشوند؟
اگرچه انجام این تست برای تمام زنان باردار مفید است، اما در شرایط زیر بهطور ویژه توصیه میشود:
- سن مادر بالای ۳۵ سال
- وجود سابقه خانوادگی اختلالات کروموزومی
- نتیجه غیرطبیعی در تستهای غربالگری سهماهه اول یا دوم
- سابقه بارداری قبلی با ناهنجاری کروموزومی
- نتایج سونوگرافی مشکوک
- بارداری حاصل از روشهای کمکباروری (IVF)
جمعبندی
تست سل فری دیانای (cfDNA / NIPT) گامی بزرگ در پیشرفت علم ژنتیک و مراقبتهای دوران بارداری است. این آزمایش بدون هیچ خطر یا تهاجمی، میتواند با دقت بسیار بالا احتمال وجود ناهنجاریهای کروموزومی در جنین را مشخص کند و به والدین و پزشک کمک کند تا تصمیمگیری آگاهانهتری درباره ادامه روند بارداری داشته باشند.
با این حال، نتیجه NIPT تشخیص قطعی نیست و در صورت مثبت شدن، انجام آزمایشهای تکمیلی تشخیصی توصیه میشود.
تفاوت تست سل فری DNA (NIPT) با غربالگریهای مرحله اول و دوم بارداری
یکی از رایجترین پرسشها در دوران بارداری است، بهویژه برای مادرانی که میخواهند بدانند کدام روش برایشان مناسبتر است.
در ادامه، بهصورت دقیق، علمی و در عین حال قابل فهم توضیح دادهایم 👇
🔬 تعریف کلی سه نوع تست
| نوع تست | نام دیگر | زمان انجام | نوع آزمایش | هدف اصلی |
|---|---|---|---|---|
| غربالگری مرحله اول | تست سهماهه اول | هفته ۱۱ تا ۱۳ بارداری | سونوگرافی NT + آزمایش خون (PAPP-A و β-hCG) | بررسی احتمال ناهنجاریهای کروموزومی اولیه |
| غربالگری مرحله دوم | تست سهماهه دوم | هفته ۱۵ تا ۱۸ بارداری | آزمایش خون (AFP، hCG، uE3، Inhibin-A) | بررسی دقیقتر احتمال تریزومیها و ناهنجاری لوله عصبی |
| تست سل فری DNA (NIPT) | cfDNA | از هفته ۱۰ بارداری به بعد | نمونهگیری خون مادر و بررسی DNA جنینی | بررسی مستقیم اختلالات کروموزومی با دقت بسیار بالا |
🧬 تفاوتهای اصلی بین NIPT و غربالگریهای سنتی
روش انجام
- غربالگریهای مرحله ۱ و ۲:
ترکیبی از آزمایش خون مادر و سونوگرافی هستند و میزان هورمونها و برخی پروتئینهای بارداری را میسنجند.
نتیجه فقط به صورت «احتمال بالا یا پایین» گزارش میشود. - NIPT (سل فری DNA):
در این روش، خود DNA جنینی که در خون مادر وجود دارد، با فناوری ژنتیکی پیشرفته بررسی میشود.
این یعنی تست بهجای بررسی غیرمستقیم هورمونها، مستقیماً ماده ژنتیکی جنین را میسنجد.
دقت و خطا
| تست | دقت برای سندرم داون | احتمال نتیجه اشتباه (False Positive) |
|---|---|---|
| غربالگری مرحله اول | حدود ۸۵٪ | ۵٪ |
| غربالگری مرحله دوم | حدود ۸۰٪ | ۵٪ |
| سل فری DNA (NIPT) | بیش از ۹۹٪ | کمتر از ۰٫۱٪ |
🔹 بنابراین NIPT بسیار دقیقتر است و احتمال خطای آن بسیار کمتر از غربالگریهای معمول است.
تهاجمی بودن و ایمنی
- هر سه تست غیرتهاجمی هستند (نیازی به ورود به رحم یا نمونهگیری از جنین ندارند).
- اما اگر نتیجه غربالگریهای مرحله اول یا دوم مشکوک باشد، معمولاً پزشک برای اطمینان، انجام آمنیوسنتز یا CVS را توصیه میکند.
درحالیکه اگر نتیجه NIPT منفی باشد، اغلب نیازی به تست تهاجمی نیست.
زمان و سرعت نتیجه
- غربالگری مرحله اول: حدود هفته ۱۱ تا ۱۳
- غربالگری مرحله دوم: هفته ۱۵ تا ۱۸
- NIPT: از هفته ۱۰ قابل انجام است و معمولاً نتیجه طی ۷ تا ۱۰ روز آماده میشود.
بنابراین NIPT زودتر و سریعتر میتواند اطلاعات دقیقتری در اختیار مادر قرار دهد.
هزینه
- هزینه NIPT معمولاً بالاتر از غربالگریهای معمول است، زیرا فناوری آن جدیدتر و پیچیدهتر است.
- با این حال، با توجه به دقت بسیار بالا، میتواند از انجام تستهای پرخطر و پرهزینه بعدی (مثل آمنیوسنتز) جلوگیری کند.
موارد توصیهشده برای هر تست
- برای همه مادران، غربالگری مرحله اول حداقل توصیه میشود.
- تست NIPT معمولاً برای مادرانی پیشنهاد میشود که:
- سن بالای ۳۵ سال دارند،
- نتیجه غربالگری اولیهشان مشکوک بوده،
- سابقه خانوادگی اختلالات کروموزومی دارند،
- یا میخواهند با اطمینان بالا از سلامت کروموزومی جنین مطمئن شوند.
🧩 خلاصه تفاوتها در یک نگاه
| ویژگی | غربالگری مرحله ۱ و ۲ | تست سل فری DNA (NIPT) |
|---|---|---|
| نوع بررسی | سطح هورمونها و سونوگرافی | DNA جنین در خون مادر |
| دقت | متوسط | بسیار بالا |
| احتمال خطا | نسبتاً زیاد | بسیار کم |
| زمان انجام | هفتههای ۱۱ تا ۱۸ | از هفته ۱۰ به بعد |
| هزینه | کمتر | بیشتر |
| نیاز به تست تکمیلی | در صورت مشکوک بودن نتیجه زیاد است | در اکثر موارد نیازی نیست |
| تعیین جنسیت جنین | ندارد | دارد (در صورت درخواست) |
آیا پس از انجام سل فری دیگر نیازی به انجام غربالگریهای اول و دوم نیست؟
این یکی از رایجترین پرسشها در میان مادران باردار است که تست سل فری DNA (NIPT) را انجام دادهاند یا قصد انجام آن را دارند.
پاسخ کوتاه این است:
✅ در بیشتر موارد، اگر تست سل فری DNA (NIPT) با نتیجه طبیعی و مطمئن انجام شود، دیگر نیازی به انجام غربالگریهای مرحله اول و دوم نیست.
اما توضیح دقیقترش کمی مهمتر است، چون بستگی به شرایط فردی هر مادر دارد 👇
🧬 تفاوت نقش تست سل فری و غربالگریهای سنتی
برای درک بهتر، باید بدانیم که هدف کلی غربالگریهای بارداری شناسایی خطر ناهنجاریهای کروموزومی و برخی مشکلات ساختاری جنین است.
اما هر تست، محدودهی خاصی از مشکلات را بررسی میکند:
| نوع تست | نوع اطلاعاتی که ارائه میدهد |
|---|---|
| NIPT (سل فری DNA) | بررسی احتمال اختلالات کروموزومی (مثل سندرم داون، تریزومی ۱۳، ۱۸ و اختلالات جنسی) با دقت بسیار بالا |
| غربالگری مرحله اول (سهماهه اول) | بررسی احتمال ناهنجاریهای کروموزومی + بررسی ساختار اولیه جنین با سونوگرافی NT |
| غربالگری مرحله دوم (سهماهه دوم) | بررسی هورمونهای خونی + احتمال ناهنجاری لوله عصبی (مثل اسپینا بیفیدا) |
🔹 پس از انجام NIPT چه باید کرد؟
✅ اگر نتیجه NIPT طبیعی باشد:
- معمولاً نیازی به انجام تستهای غربالگری مرحله اول و دوم نیست.
- اما هنوز باید سونوگرافیهای زمانبندیشده را انجام دهید، چون NIPT فقط اختلالات کروموزومی را بررسی میکند، نه نقصهای ساختاری (مثل مشکلات قلب، مغز یا اندامها).
بهویژه سونوگرافی NT (هفته ۱۱ تا ۱۳) و آنومالی اسکن (هفته ۱۸ تا ۲۲) همچنان ضروری هستند.
⚠️ اگر نتیجه NIPT مشکوک یا مثبت باشد:
- باید برای تأیید نهایی، یکی از تستهای تشخیصی مانند:
- آمنیوسنتز
- یا نمونهگیری از پرزهای جفتی (CVS)
انجام شود.
⚖️ نکته مهم:
برخی پزشکان (از جمله متخصصان زنان و زایمان در ایران) همچنان توصیه میکنند حتی پس از NIPT،
سونوگرافی NT سهماهه اول انجام شود،
چون ممکن است برخی ناهنجاریهای غیرکروموزومی در NIPT مشخص نشوند، اما در سونوگرافی دیده شوند.
💬 جمعبندی نهائی
| سؤال | پاسخ |
|---|---|
| آیا پس از انجام NIPT باید غربالگری مرحله اول انجام شود؟ | در اغلب موارد، خیر؛ ولی انجام سونوگرافی NT همچنان توصیه میشود. |
| آیا نیاز به غربالگری مرحله دوم هست؟ | معمولاً خیر، مگر پزشک بر اساس شرایط خاص مادر توصیه کند. |
| آیا NIPT همه چیز را بررسی میکند؟ | خیر، فقط اختلالات کروموزومی را؛ نه ناهنجاریهای ساختاری یا مشکلات ارگانها. |
| آیا انجام NIPT کافی است؟ | اگر با سونوگرافی NT و آنومالی اسکن ترکیب شود، بله، برای بیشتر مادران کافی است. |
🩺 توصیه نهائی:
اگر قصد دارید تست سل فری DNA (NIPT) انجام دهید، بهترین رویکرد این است که:
- در هفته ۱۱ تا ۱۳: سونوگرافی NT انجام دهید.
- از هفته ۱۰ به بعد: تست NIPT را انجام دهید.
- در هفته ۱۸ تا ۲۲: سونوگرافی آنومالی دقیق جنین را انجام دهید.
به این ترتیب، هم سلامت ژنتیکی و هم ساختاری جنین با بالاترین دقت ممکن بررسی میشود.
نام قدیمی بیماریها | معرفی ۱۵ بیماری
نام قدیمی بیماریها موضوع مورد بحث این مقاله از سایت دکتر ابوئی است. در ادامه همراه ما باشید. در طول تاریخ، بسیاری از بیماریها نامهایی داشتهاند که امروز برای ما عجیب و ناآشنا هستند. مردم در گذشته بر اساس ظاهر، علائم یا باورهای سنتی، برای هر بیماری نام خاصی میگذاشتند. با پیشرفت علم پزشکی، این نامها تغییر کردند و جای خود را به اصطلاحات علمی امروزی دادند.
در این مقاله، فهرستی از بیماریهایی که در قدیم اسم دیگری داشتند آوردهایم تا با ریشهی تاریخی و زبانی آنها آشنا شوید.
نام قدیمی بیماریها
۱. حَناق → دیفتری (Diphtheria)
در متون کهن فارسی و عربی، «حناق» به بیماریای گفته میشد که باعث ورم شدید گلو و خفگی میشد. این نام از واژهی عربی به معنی «خفهکننده» آمده است.
امروزه این بیماری با نام علمی دیفتری شناخته میشود که عامل آن باکتری Corynebacterium diphtheriae است. خوشبختانه با واکسن دیفتری، این بیماری تقریباً ریشهکن شده است.
۲. کوفت : نام قدیمی بیماری آنفلوآنزا یا ویروسهای فصلی
وقتی در گذشته کسی دچار بدندرد، تب و بیحالی میشد، مردم میگفتند «کوفت شده است». این واژه از حس کوبیدگی بدن گرفته شده است.
در واقع بیشتر این موارد همان آنفلوآنزا یا ویروسهای فصلی بودند که باعث درد عضلات میشوند. هنوز هم مردم میگویند: «بدنم کوفته است».
۳. وبا → عفونت رودهای ناشی از باکتری وبا
در قدیم، هر نوع اسهال و استفراغ شدید را «وبا» مینامیدند. بعدها مشخص شد وبا بیماری خاصی است که از طریق آب آلوده منتقل میشود و عامل آن باکتری Vibrio cholerae است.
در ادبیات فارسی، وبا نماد مرگ ناگهانی و بلای عمومی است، مثل بیت معروف حافظ:
در این زمانهی آلوده، وبا خوشتر از هواست.
۴. تب نوبه → مالاریا
«تب نوبه» در طب سنتی به تبهایی گفته میشد که در زمانهای منظم تکرار میشدند، مثل یکروز در میان.
امروزه میدانیم این الگوی تب مربوط به مالاریا است که توسط پشهی آنوفل منتقل میشود. واژهی «نوبه» در عربی به معنی «نوبت» است و اشاره به تناوب تب دارد.
۵. قولنج → کولیک (Colic)
قولنج در زبان عامیانه به هر نوع درد پیچشی در شکم یا پهلو گفته میشد. در طب مدرن، بسته به ناحیه، میگویند:
- قولنج صفراوی (سنگ صفرا)
- قولنج کلیوی (سنگ کلیه)
- قولنج رودهای (گرفتگی روده)
۶. ذاتالجَنب → التهاب پردهی جنب (Pleurisy)
ذاتالجنْب بیماریای بود که با تب، درد پهلو و تنگی نفس همراه میشد. در واقع همان التهاب پردهی جنب یا ریه است. در برخی متون، آن را با ذاتالریه (پنومونی) اشتباه میگرفتند.
۷. تب نَسّی یا تب خشک → سل (Tuberculosis)
قبل از شناخت میکروب سل، مردم بیماری را که موجب لاغری، سرفههای خشک و تب مداوم میشد، «تب نسی» مینامیدند.
رابرت کخ در قرن نوزدهم علت این بیماری را کشف کرد: باکتری Mycobacterium tuberculosis.
۸. مالیخولیا → افسردگی یا اختلالات روانی
در طب قدیم، مالیخولیا بیماریای بود که فرد را غمگین، بدبین و گوشهگیر میکرد. پزشکان قدیم آن را نتیجهی «غلبهی سودا» میدانستند.
در روانپزشکی امروز، معادل آن افسردگی، سایکوز یا اختلال دوقطبی است.
دریافت نوبت مطب دکتر ابوئی در فردیس
۹. خنازیر → آبسه یا غدد چرکی گردن
«خنازیر» به تورمهای دردناک و چرکی گردن گفته میشد. معمولاً ناشی از عفونت غدد لنفاوی بود.
در گذشته مردم برای درمان خنازیر از حجامت یا داروهای گیاهی استفاده میکردند، اما امروزه با آنتیبیوتیک درمان میشود.
۱۰. جُدَری → آبله (Smallpox)
«جدری» همان آبله است، بیماریای که قرنها جان میلیونها نفر را گرفت.
این بیماری با واکسیناسیون جهانی بهطور کامل ریشهکن شد. واژهی «آبله» در فارسی از تاولهای پرآب آن گرفته شده است.
۱۱. طاعون → Plague
طاعون در گذشته بلایی خانمانسوز بود که جمعیت زیادی را از بین برد. عامل آن باکتری Yersinia pestis است.
در زبان فارسی، «مرگ سیاه» یا «وبا» نیز گاهی برای طاعون بهکار میرفت.
۱۲. جذام → بیماری هانسن (Leprosy)
جذام بیماریای مزمن و مسری بود که پوست و اعصاب را درگیر میکرد. در قرون وسطی بیماران جذامی از جامعه طرد میشدند.
امروزه میدانیم عامل آن باکتری Mycobacterium leprae است و درمان دارد.
۱۳. سرسام → مننژیت یا التهاب مغز
در گذشته، هر بیماریای که باعث تب بالا، سردرد و گیجی میشد را «سرسام» مینامیدند.
امروزه این علائم معمولاً مربوط به مننژیت (التهاب پردههای مغز) یا انسفالیت (التهاب بافت مغزی) هستند.
۱۴. دق → افسردگی شدید یا نارسایی اندامها بر اثر غم
در ادبیات فارسی زیاد میخوانیم: «از غم دق کرد».
در گذشته، دق به بیماریای گفته میشد که فرد از شدت غصه یا اندوه بیمار و نحیف میشد و میمرد. امروزه این حالت را معادل افسردگی شدید یا نارسایی ناشی از استرس مزمن میدانند.
۱۵. داءالکلب → هاری (Rabies)
«داءالکلب» در زبان عربی به معنی «بیماری سگ» است. در متون کهن فارسی و طب سنتی، این نام برای هاری استفاده میشد.
عامل آن ویروسی است که از طریق گاز گرفتن حیوان آلوده منتقل میشود.
🧩 جمعبندی: چرا شناخت نامهای قدیمی بیماریها مهم است؟
شناخت نامهای قدیمی بیماریها فقط از نظر زبانی جالب نیست، بلکه به درک بهتر تاریخ پزشکی، ادبیات فارسی و فرهنگ عامه کمک میکند.
وقتی در اشعار حافظ یا سعدی واژههایی مانند «دق»، «وبا»، «قولنج» یا «مالیخولیا» میخوانیم، میتوانیم بفهمیم منظور شاعران چه بوده است.
همچنین این واژهها نشان میدهند که مردم چگونه بیماریها را درک میکردند و علم پزشکی چه مسیری را طی کرده تا به امروز برسد.